Détails du sujet
Chimie thérapeutique
Nom ? Classe Thérapeutique ? Classe Chimique ? Cible ? Mécanisme d'action ?
Toutes les cartes
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
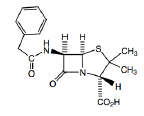
Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Pénicilline hémisynthétique
Pénicilline G Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
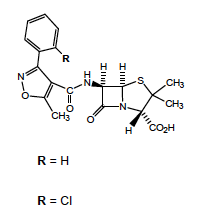
Oxacilline et Cloxacilline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : PENICILLINES M : ISOXAZOLYLPENICILLINES
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane

Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
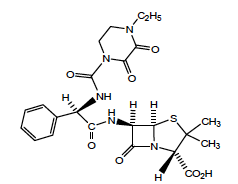
Pipéracilline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : UREIDOPENICILLINE
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
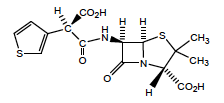
Ticarcilline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CARBOXYPENICILLINES Pénicilline hémisynthétique
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?

Pipéracilline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : UREIDOPENICILLINE
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
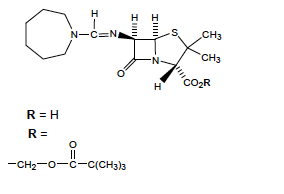
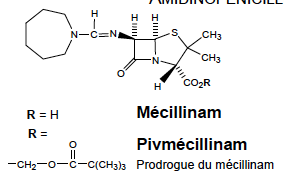
Mécillinam - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Aminidopénicilline
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
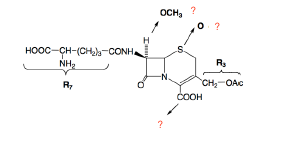
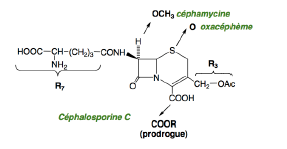
Céfalosporine C - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE PREMIERE GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
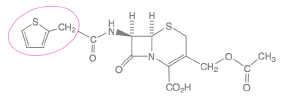
C1G Céfalotine voie parentérale - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE PREMIERE GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
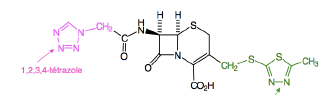
C1G Céfazoline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE PREMIERE GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
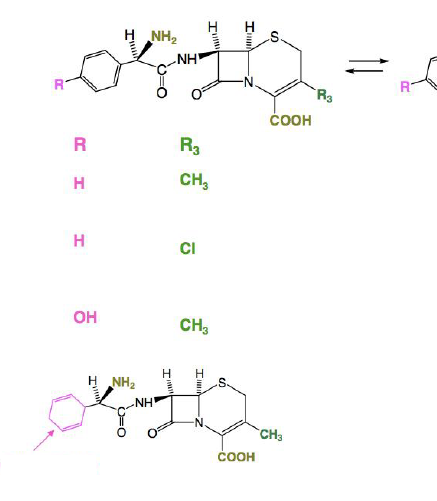
Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE PREMIERE GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
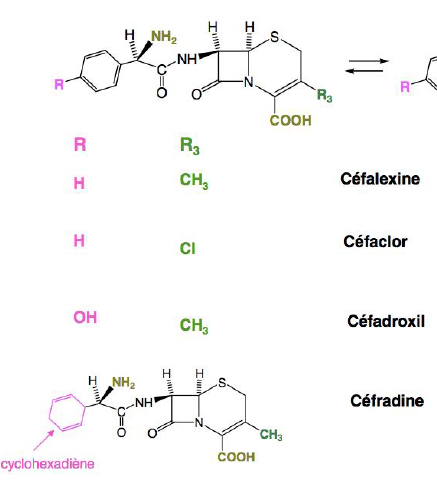
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
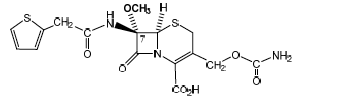
C1G voie orale - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE DEUXIEME GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
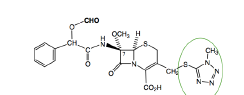
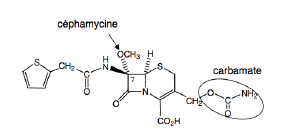
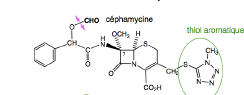
C2G Céfamandole - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE DEUXIEME GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
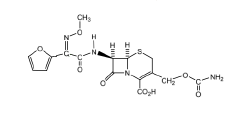
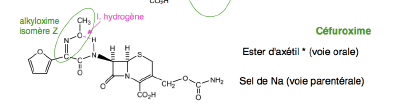
C2G Céfuroxime - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE DEUXIEME GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
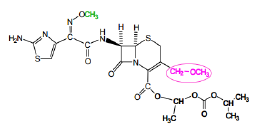
C3G Cefpodoxime - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE TROISIEME GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
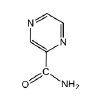
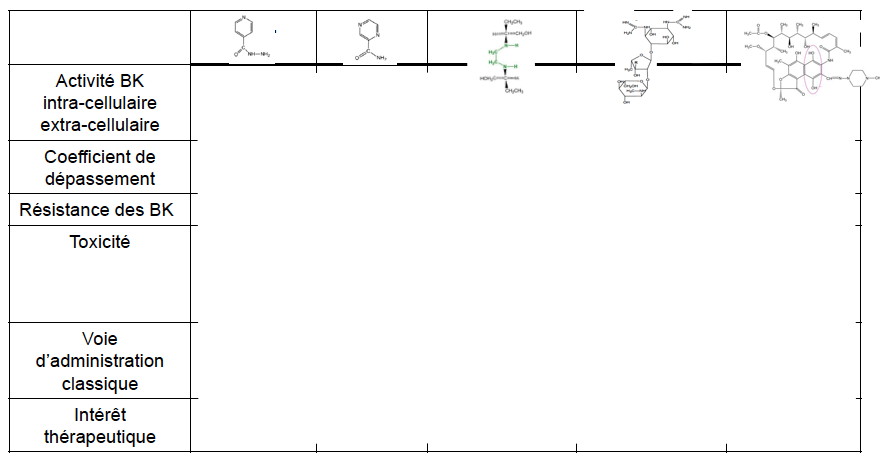
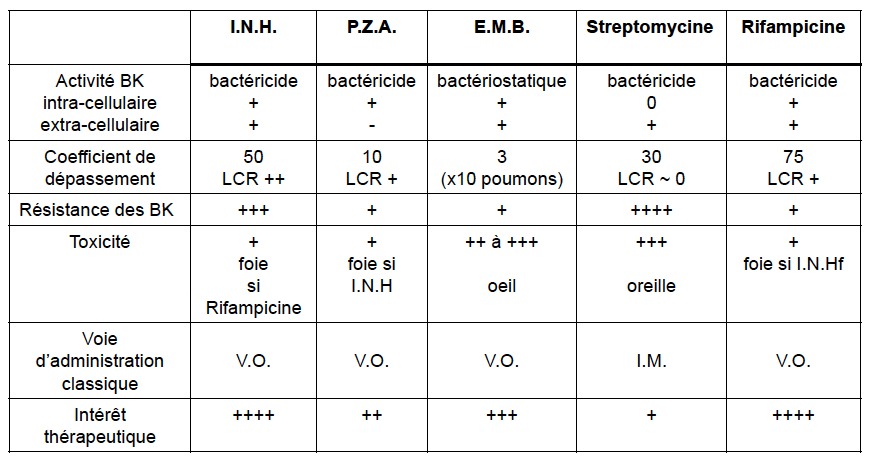
Pyrazinamide - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antituberculeux de synthèse
Cible : Paroi bactérienne
Mécanisme d'action : Celui-ci pénètre dans la bactérie. Une fois dedans, il semblerait qu’il interfère avec la synthèse des acide mycoliques (constituants de la paroi du bacille de Koch), sans doute en inhibant un acide gras synthétase de type I.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
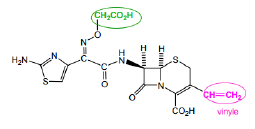
C3G Céfixime Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE TROISIEME GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
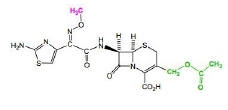
C3G Céfotaxime - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : CEPHALOSPORINES DE TROISIEME GENERATION
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
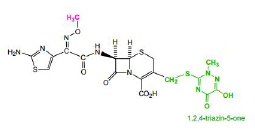
C3G Voie parentérale : Ceftriaxone - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Céphalosporine
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
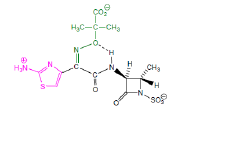
Aztréonam - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Monobactame
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
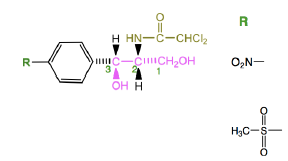
Thiamphénicol - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Phénicolés
Cible : Synthèse protéique
Mécanisme d'action : Bloquent la synthèse des protéines en se fixant sur les ribosomes par inhibition de la peptidyltransférase.
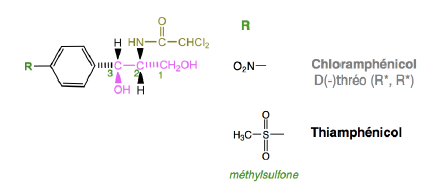
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
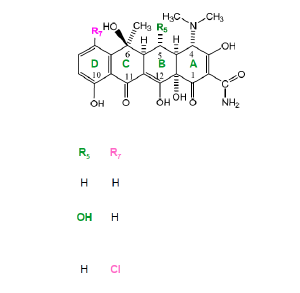
Tétracycline 1G - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Tétracyclines
Cible : Synthèse protéique
Mécanisme d'action : Bloquent la synthèse des protéines en se fixant sur les ribosomes par inhibition de la peptidyltransférase.
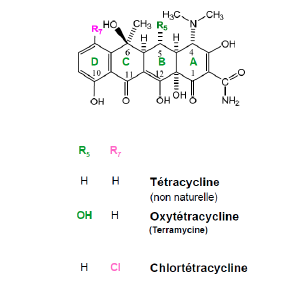
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
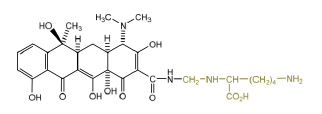
Tétracycline 2G : Lymécycline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Tétracyclines hémisynthétiques
Cible : Synthèse protéique
Mécanisme d'action : Bloquent la synthèse des protéines en se fixant sur les ribosomes par inhibition de la peptidyltransférase.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
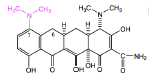
Tétracycline 2G : Minocycline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Tétracyclines
Cible : Synthèse protéique
Mécanisme d'action : Bloquent la synthèse des protéines en se fixant sur les ribosomes par inhibition de la peptidyltransférase.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
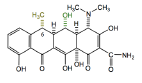
Tétracycline 3G : Doxycycline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Tétracyclines
Cible : Synthèse protéique
Mécanisme d'action : Bloquent la synthèse des protéines en se fixant sur les ribosomes par inhibition de la peptidyltransférase.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
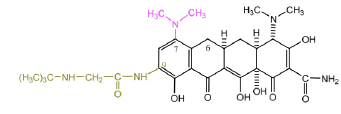
Tétracycline 4G : Tigécycline - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Tétracyclines
Cible : Synthèse protéique
Mécanisme d'action : Bloquent la synthèse des protéines en se fixant sur les ribosomes par inhibition de la peptidyltransférase.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
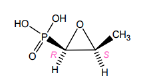
Fosfomycine - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Fosfomycine
Cible : Paroi bactérienne
Mécanisme d'action :La Fosfomycine agit sur la Pyruvyl transférase qui est chargé de catalyser la réaction entre la PEP et l’UDP-NAG (N-acetyl-glucosamine) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
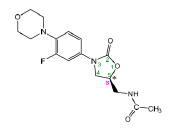
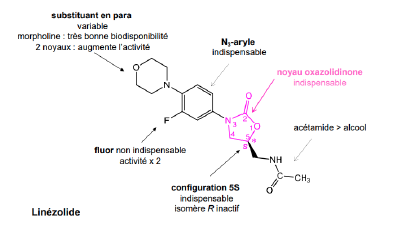
Linézolide - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Oxazolidinones
Cible : Synthèse protéique
Mécanisme d'action : Agit en se fixant sur la sous unité 50S des ribosomes ce qui empêche la formation du complexe 70S. Cette fixation induit donc une impossibilité de synthétiser les protéines.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
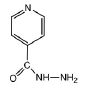
Isoniazide - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antituberculeux de synthèse
Mécanisme d'action : L’isoniazide est métabolisé par KatG donnant un radical isonicotinique puis on observe une réduction mono-électrique grâce au NAD+ conduisant à un adduit INH-NAD(H). Celui-ci inhibe l’enzyme InhA (énoyl-ACP réductase) bloquant la synthèse des acides mycoliques, perturbant ainsi la paroi du bacille de Koch.
Il est possible d’avoir un deuxième mécanisme qui se passe en même temps toujours par KatG en présence d’eau oxygénée (H2O2) donnant un radical qui sera peroxydé et à terme génèrera de l’oxyde nitrique, un réactif toxique pour la bactérie.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?

Thiamphénicol - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Phénicolés
Cible : Synthèse protéique
Mécanisme d'action : Bloquent la synthèse des protéines en se fixant sur les ribosomes par inhibition de la peptidyltransférase.

Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
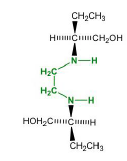
Ethambutol - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antituberculeux de synthèse
Mécanisme d'action : La chélation avec ces métaux va être responsable d’effets indésirables et va être impliqué dans le mécanisme d’action de la molécule. Le chélate de zinc ou de cuivre perturbe la biosynthèse des arabinogalactanes et des lipoarabinomannanes, composants la paroi des bacilles de Koch, en inhibant une enzyme l’arabinosyltransférase III.
Classe Thérapeutique ?
Classe Chimique ?
Mécanisme d'action ?
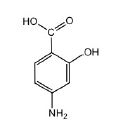
Acide para-aminosalicylique - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antituberculeux de synthèse
Mécanisme d'action : Cette molécule est métabolisée au niveau du foie pour donner un dérivé N-acétylé, potentiellement hépatotoxique. On ne sait pas trop comment elle agit, sans doute en limitant la synthèse des folates ou en inhibant la dihydroptéroate réductase (analogie structurale avec l’acide para-aminobenzoïque).
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
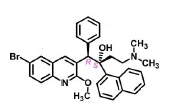
Bédaquiline - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antituberculeux de synthèse
Famille : Diatylquinoléines
Mécanisme d'action :
elle inhibe l’ATP synthase. Cette enzyme permet de fournir une source d’énergie pour la bactérie, ainsi si on l’inhibe on enlève cette source d’énergie et donc a un effet bactéricide. Cette action est due à une migration de protons, on observe un ancrage de la bédaquiline dans l’ATP synthétase.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
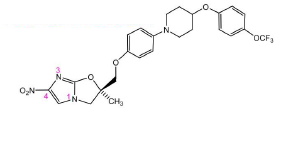
Delamanide - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antituberculeux de synthèse
Famille : 4-nitroimidazoles
Mécanisme d'action : Agit sur la synthèse d’acide mycolique. Donc on retrouve la même cible à long terme de l’isoniazide et la Pyrazinamide. Mais la délamanide agit sur les acides méthoxy- et cétomycolqiues.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
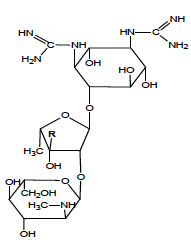
Streptomycine - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antibiotiques antituberculeux
Mécanisme d'action : Elle se lie à l'ARN ribosomique 16S de la sous-unité ribosomique 30S du ribosome bactérien, en interférant avec la liaison de l'ARNt de la N-Formylméthionine à la sous-unité 30S. Cette interférence peut conduire à des lectures erronées de codons, l'inhibition de la synthèse de protéines et entrainer la mort de la cellule microbienne
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
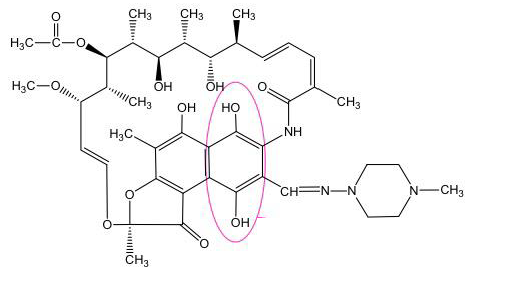
Rifampicine - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antibiotiques antituberculeux DERIVES DE LA RIFAMYCINE
Mécanisme d'action : Cette molécule va inhiber la synthèse d’ARN, elle est active à la fois sur le bacille de Koch et le bacille de la lèpre en se liant à ARN polymérase formant un complexe stable. Elle est bactéricide, active sur les deux types de bacille (intra/extra)
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
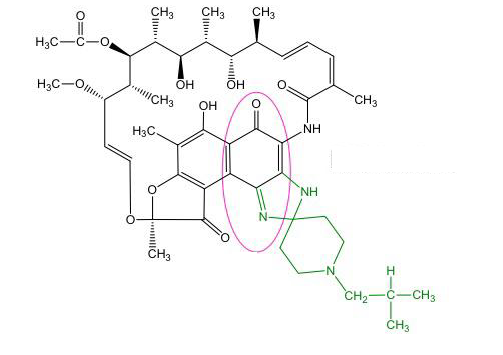
Rifabutine - Classe Thérapeutique : Antimycobactériens
Classe Chimique : Antibiotiques antituberculeux DERIVES DE LA RIFAMYCINE
Mécanisme d'action : Cette molécule va inhiber la synthèse d’ARN, elle est active à la fois sur le bacille de Koch et le bacille de la lèpre en se liant à ARN polymérase formant un complexe stable. Elle est bactéricide, active sur les deux types de bacille (intra/extra)
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
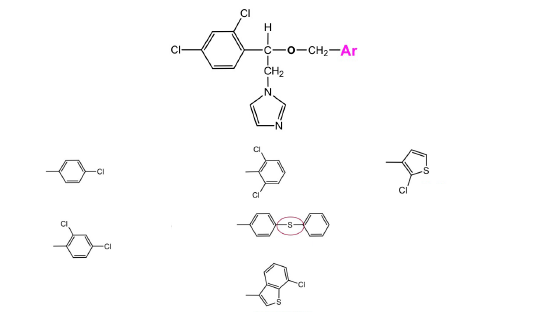
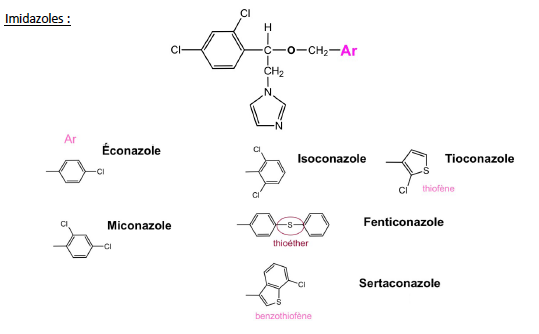
Imidazoles - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : Conazoles et analogues
Famille chimique : Imidazoles
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
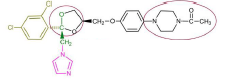
Kétoconazole - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : Conazoles et analogues
Famille chimique : Imidazoles
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
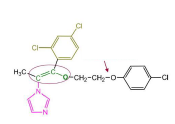
Omoconazole - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : Conazoles et analogues
Famille chimique : Imidazoles
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
Oxiconazole - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : Conazoles et analogues
Famille chimique : Imidazoles
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
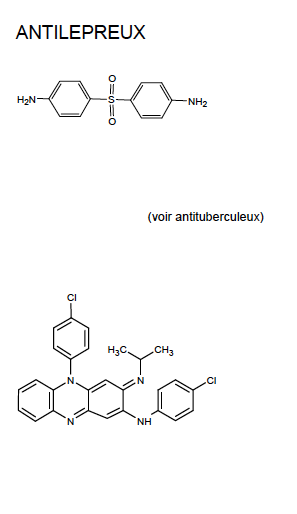
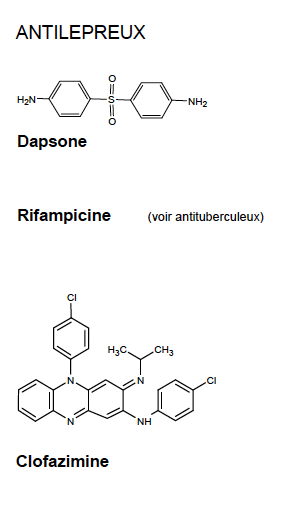
Dapsone et clofazimine - Classe Thérapeutique : Antimycobactériens
Classe Chimique : ANTILEPREUX
Mécanisme d'action : Cette molécule va inhiber la synthèse d’ARN, elle est active à la fois sur le bacille de Koch et le bacille de la lèpre en se liant à ARN polymérase formant un complexe stable. Elle est bactéricide, active sur les deux types de bacille (intra/extra)
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
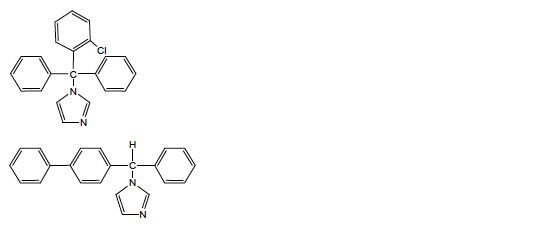
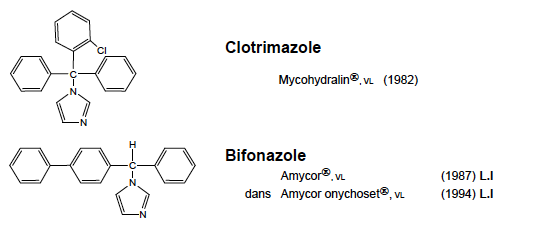
Clotrimazole Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : - Conazoles et analogues
Famille chimique : Imidazoles
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
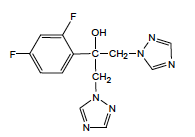
Fluconazole - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : Conazoles et analogues
Famille chimique : TRIAZOLES
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
Voriconazole - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : Conazoles et analogues
Famille chimique : TRIAZOLES
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
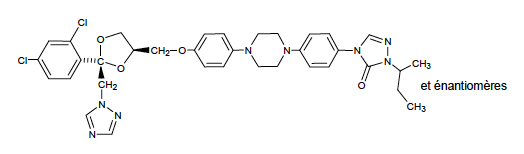
Itraconazole - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : Conazoles et analogues
Famille chimique : TRIAZOLES
Mécanisme d'action : Les imidazoles agissent sur la synthèse de l’ergostérol qui est un des constituants importants de la paroi des champignons. Ces dérivés azolés inhibent une enzyme : la 14 α-déméthylase à sélectivité importante (pas spécifique) en inhibant le cytochrome CYP par complexation du fer.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
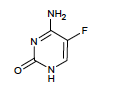
Flucytosine - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : AUTRES ANTIFONGIQUES A ACTION SYSTEMIQUE
Mécanisme d'action : La 5-Fluorocytosine pénètre dans la paroi des champignons grâce à un transporteur actif, une fois entrée dans la cellule, elle subit une désamination par une cytosine-desaminase (enzyme spécifique des champignons) pour donner le 5-Fluorouracile(=5-FU). Il y aura ensuite, introduction d’un ribose ou d’un désoxyribose qui va être phosphorylé et intégré dans la synthèse de l’ARN fongique (le 5-FU est un antimétabolite).
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
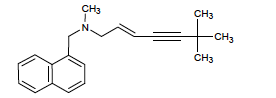
Terbinafine - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : ALLYLAMINE - AUTRES ANTIFONGIQUES A ACTION SYSTEMIQUE
Il agit sur une étape qui n’est pas spécifique à la synthèse de la paroi fongique.Il est utilisé pour traiter les onychomycoses.Utilisation par voie locale sous forme de vernis mais si insuffisant, il faut passer par une phase systémique : lors d’une utilisation par voie orale, elle va avoir un tropisme pour l’ongle.Il peut être aussi sous forme d’un gel pour traiter les « pieds d’athlètes » (infections attrapées lors de sueurs intenses dans les baskets)
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
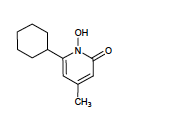
Ciclopirox - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : AUTRES ANTIFONGIQUES A ACTION topique
Mécanisme d'action : possibilité de chélation de métaux d’où le mécanisme de ce composé: inhibition des enzymes fongiques ayant besoin de métaux pour fonctionner.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
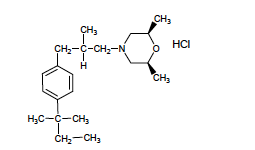
amorolfine - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : AUTRES ANTIFONGIQUES A ACTION topique
Mécanisme d'action : elle agit après la différenciation du lanostérol donc sur 2 enzymes : une réductase et une isomérase, provoque donc une perturbationde la synthèse de l’ergostérol et donc de la paroi cellulaire des champignons.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
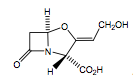
Acide clavulanique - Classe Thérapeutique : Antibactérien de synthèse à action systémique
Classe Chimique : HETEROCYCLES NITRES - NITROFURANES
Cible : ADN
Mécanisme d'action : Deux réductions donnent un dérivé nitrosé qui va former des adduits à l’ADN. Une troisième réduction va donner l’hydroxylamine qui forme également des adduits à l’ADN. En présence d’O2, on a une réduction du dérivé nitrosé qui va former un ion superoxyde, qui lui-même forme un radical hydroxyle qui casse l’ADN. L’action est sélective voir spécifique aux bactéries : les nitroréductases bactériennes réduisent le nitrofurane.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
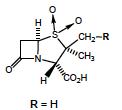
Sulbactam - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique :BETA-LACTAMINES HEMISYNTHETIQUES - INHIBITEURS DE ß-LACTAMASES
Cible : ß-lactamases
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
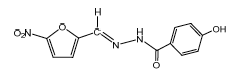
Nifuroxazide - Classe Thérapeutique : Antibactérien de synthèse à action systémique
Classe Chimique : HETEROCYCLES NITRES - NITROFURANES
Cible : ADN
Mécanisme d'action : Deux réductions donnent un dérivé nitrosé qui va former des adduits à l’ADN. Une troisième réduction va donner l’hydroxylamine qui forme également des adduits à l’ADN. En présence d’O2, on a une réduction du dérivé nitrosé qui va former un ion superoxyde, qui lui-même forme un radical hydroxyle qui casse l’ADN. L’action est sélective voir spécifique aux bactéries : les nitroréductases bactériennes réduisent le nitrofurane.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
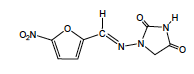
Nitrofurantoïne - Classe Thérapeutique : Antibactérien de synthèse à action systémique
Classe Chimique : HETEROCYCLES NITRES - NITROFURANES
Cible : ADN
Mécanisme d'action : Deux réductions donnent un dérivé nitrosé qui va former des adduits à l’ADN. Une troisième réduction va donner l’hydroxylamine qui forme également des adduits à l’ADN. En présence d’O2, on a une réduction du dérivé nitrosé qui va former un ion superoxyde, qui lui-même forme un radical hydroxyle qui casse l’ADN. L’action est sélective voir spécifique aux bactéries : les nitroréductases bactériennes réduisent le nitrofurane.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
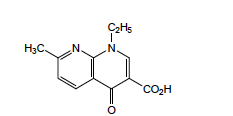
Acide Nalidixique - Classe Thérapeutique : Antibactérien de synthèse à action systémique Classe Chimique : QUINOLONES DE PREMIERE GENERATION Cible : ADN
Mécanisme d'action : Les cibles de ces composés sont les topoisomérases II et IV. La topoisomérase II est spécifique aux bactéries et est aussi appelée l’ADN gyrase. Ce sont les enzymes clés de la réplication de l’ADN bactérien qui coupent 1 ou 2 brins de l’ADN. Elles sont constituées de 2 sous-unités dimériques et symétriques. On parle des sous unités gyrA et gyrB pour l’ADN gyrase et parC et parE pour la topoisomérase IV. Les quinolones se fixent donc à l’interface de ces 2 sous-unités pour chaque enzyme mais seulement quand ces enzymes sont déjà fixées à l’ADN et l’ont déjà coupé. D’une manière générale, les quinolones se fixant sur l’ADN gyrase ont une activité sur les bactéries gram- et celles se fixant sur la topoisomérase IV ont sur activité sur les bactéries gram+. Il y a donc formation d’un complexe très stable : ADN-Quinolone-Gyrase/Topoisomérase IV qui responsable de l’effet bactéricide.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
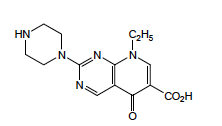
Acide Pipémidique - Classe Thérapeutique : Antibactérien de synthèse à action systémique Classe Chimique : QUINOLONES DE PREMIERE GENERATION Cible : ADN
Mécanisme d'action : Les cibles de ces composés sont les topoisomérases II et IV. La topoisomérase II est spécifique aux bactéries et est aussi appelée l’ADN gyrase. Ce sont les enzymes clés de la réplication de l’ADN bactérien qui coupent 1 ou 2 brins de l’ADN. Elles sont constituées de 2 sous-unités dimériques et symétriques. On parle des sous unités gyrA et gyrB pour l’ADN gyrase et parC et parE pour la topoisomérase IV. Les quinolones se fixent donc à l’interface de ces 2 sous-unités pour chaque enzyme mais seulement quand ces enzymes sont déjà fixées à l’ADN et l’ont déjà coupé. D’une manière générale, les quinolones se fixant sur l’ADN gyrase ont une activité sur les bactéries gram- et celles se fixant sur la topoisomérase IV ont sur activité sur les bactéries gram+. Il y a donc formation d’un complexe très stable : ADN-Quinolone-Gyrase/Topoisomérase IV qui responsable de l’effet bactéricide.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
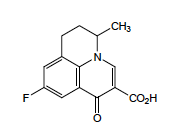
Fluméquine - Classe Thérapeutique : Antibactérien de synthèse à action systémique Classe Chimique : QUINOLONES DE PREMIERE GENERATION Cible : ADN
Mécanisme d'action : Les cibles de ces composés sont les topoisomérases II et IV. La topoisomérase II est spécifique aux bactéries et est aussi appelée l’ADN gyrase. Ce sont les enzymes clés de la réplication de l’ADN bactérien qui coupent 1 ou 2 brins de l’ADN. Elles sont constituées de 2 sous-unités dimériques et symétriques. On parle des sous unités gyrA et gyrB pour l’ADN gyrase et parC et parE pour la topoisomérase IV. Les quinolones se fixent donc à l’interface de ces 2 sous-unités pour chaque enzyme mais seulement quand ces enzymes sont déjà fixées à l’ADN et l’ont déjà coupé. D’une manière générale, les quinolones se fixant sur l’ADN gyrase ont une activité sur les bactéries gram- et celles se fixant sur la topoisomérase IV ont sur activité sur les bactéries gram+. Il y a donc formation d’un complexe très stable : ADN-Quinolone-Gyrase/Topoisomérase IV qui responsable de l’effet bactéricide.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
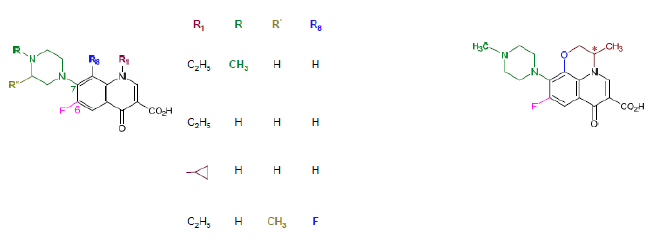
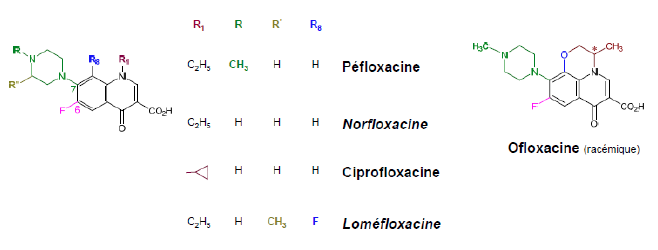
Fluoroquinolone - Classe Thérapeutique : Antibactérien de synthèse à action systémique Classe Chimique : QUINOLONES DE deuxième GENERATION - Fluoroquinolone Cible : ADN Mécanisme d'action : Les cibles de ces composés sont les topoisomérases II et IV. La topoisomérase II est spécifique aux bactéries et est aussi appelée l’ADN gyrase. Ce sont les enzymes clés de la réplication de l’ADN bactérien qui coupent 1 ou 2 brins de l’ADN. Elles sont constituées de 2 sous-unités dimériques et symétriques. On parle des sous unités gyrA et gyrB pour l’ADN gyrase et parC et parE pour la topoisomérase IV. Les quinolones se fixent donc à l’interface de ces 2 sous-unités pour chaque enzyme mais seulement quand ces enzymes sont déjà fixées à l’ADN et l’ont déjà coupé. D’une manière générale, les quinolones se fixant sur l’ADN gyrase ont une activité sur les bactéries gram- et celles se fixant sur la topoisomérase IV ont sur activité sur les bactéries gram+. Il y a donc formation d’un complexe très stable : ADN-Quinolone-Gyrase/Topoisomérase IV qui responsable de l’effet bactéricide.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
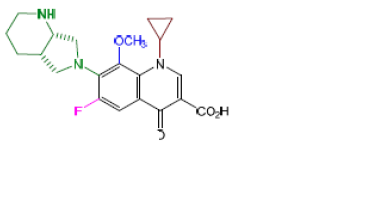
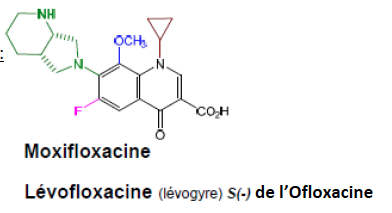
Moxifloxacine - Classe Thérapeutique : Antibactérien de synthèse à action systémique Classe Chimique : QUINOLONES DE TROISIEME GENERATION - Fluoroquinolone Cible : ADN
Mécanisme d'action : Les cibles de ces composés sont les topoisomérases II et IV. La topoisomérase II est spécifique aux bactéries et est aussi appelée l’ADN gyrase. Ce sont les enzymes clés de la réplication de l’ADN bactérien qui coupent 1 ou 2 brins de l’ADN. Elles sont constituées de 2 sous-unités dimériques et symétriques. On parle des sous unités gyrA et gyrB pour l’ADN gyrase et parC et parE pour la topoisomérase IV. Les quinolones se fixent donc à l’interface de ces 2 sous-unités pour chaque enzyme mais seulement quand ces enzymes sont déjà fixées à l’ADN et l’ont déjà coupé. D’une manière générale, les quinolones se fixant sur l’ADN gyrase ont une activité sur les bactéries gram- et celles se fixant sur la topoisomérase IV ont sur activité sur les bactéries gram+. Il y a donc formation d’un complexe très stable : ADN-Quinolone-Gyrase/Topoisomérase IV qui responsable de l’effet bactéricide.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
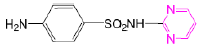
Pénicilline G - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : SULFAMIDES ET INHIBITEURS DE LA DIHYDROFOLATE REDUCTASE - S1G
Cible : ADN
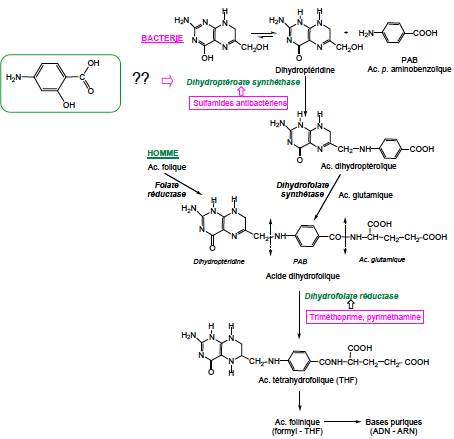
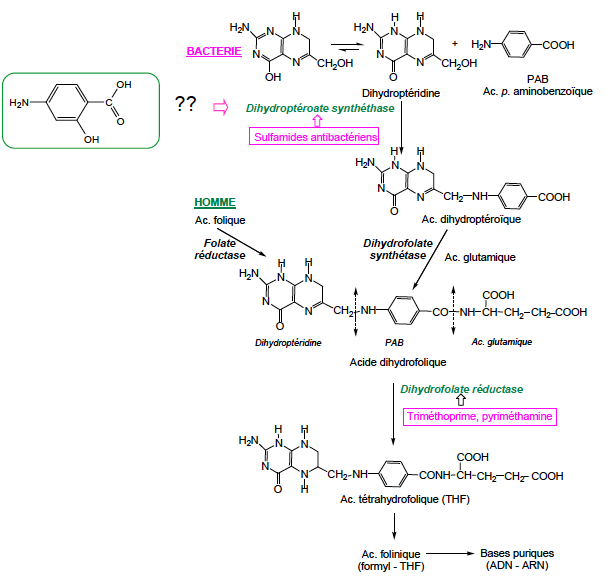
Mécanisme d'action : Chez la bactérie, l’acide dihydrofolique est synthétisé intégralement. Elle possède trois parties : la dihydroptéridine, l’acide para-aminobenzoïque et l’acide glutamique. Il existe 2 en- zymes bactériennes : la Dihydroptéroate synthéthase et la Dihydrofolate synthétase. Les sulfamides antibactériens agissent en inhibant la dihydroptéroate synthétase (inhibiteur compétitif par rapport au PAB). Cela entraine un effet bactériostatique.
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
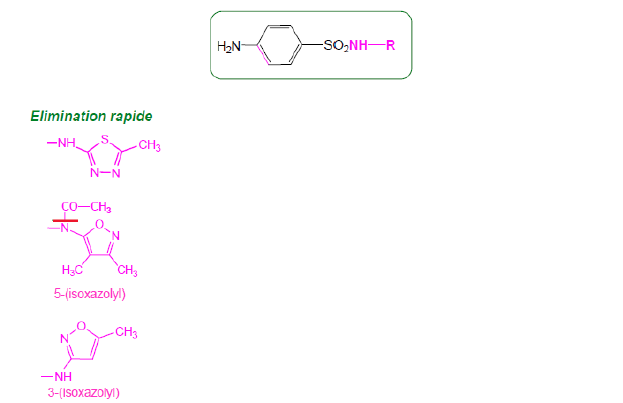
Sulfamides 2G - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : Pénicilline
Cible : Paroi bactérienne
Mécanisme d'action : se fixe aux protéines de liaison des pénicillines (PLP), transpeptidases et carboxypeptidases, responsables de la réticulation des N-acetyl-glucosamine (NAG) et l’acide N-acetylmuramique (NAM) lors de la synthèse du peptidoglycane essentiel à la membrane
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?
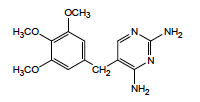
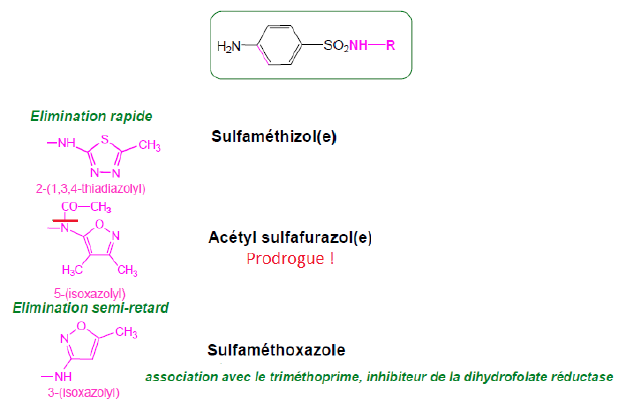
Triméthoprime - Classe Thérapeutique : Antibiotiques d’hémisynthèse
Classe Chimique : INHIBITEURS DE LA DIHYDROFOLATE REDUCTASE
Cible : ADN
Mécanisme d'action : inhibiteur de la dihydrofolate réductase
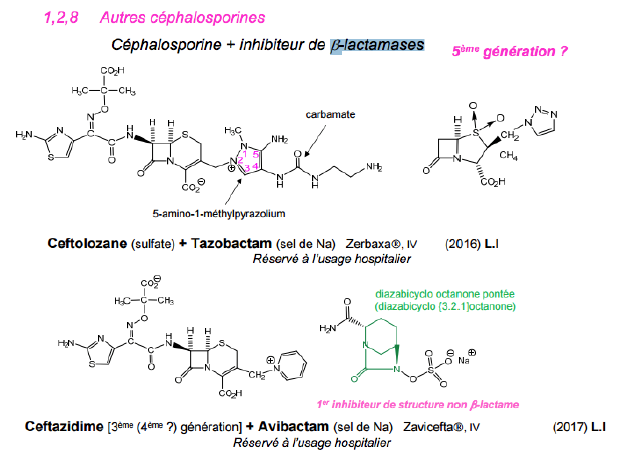
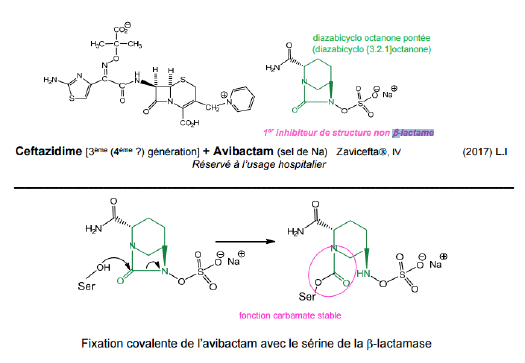
Classe Thérapeutique ?
Classe Chimique ?
Mécanisme d'action ?
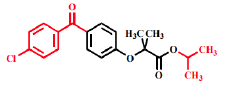
Fénofibrate - Classe Thérapeutique : Normolipémiant hypolipémiant
Classe Chimique : FIBRATES
Mécanisme d'action : Tous les fibrates sont des agonistes des PPARα (peroxysome proliferator-activated receptors). Ces récepteurs vont être capables de stimuler la transcription de gènes codant diverses protéines impliquées dans le métabolisme des lipides et des lipoprotéines.
Classe Thérapeutique ?
Classe Chimique ?
Mécanisme d'action ?
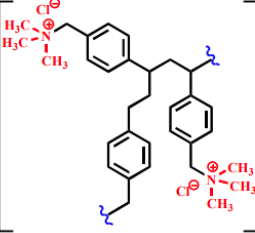
Colestyramine - Classe Thérapeutique : Normolipémiant hypolipémiant
Classe Chimique : Résine chélatrice d’acides biliaires
Mécanisme d'action : Il y piège les acides gras en les chélatant. Ce sont des résines échangeuses d’anions (anions Cl-/ acides biliaires). Elles échangent leurs sels Cl- contre les fonctions COO- des acides biliaires, et comme ces résines sont insolubles elles sont éliminées avec le cholestérol qu’elles ont piégé. Diminution du cycle entéro hépatique des acides biliaires, ils sont piégés dans la lumière intestinale, et sont donc éliminés dans les fèces au lieu d’être recaptés. Augmentation indirecte du catabolisme des acides biliaires (Cholestérol).
Classe Thérapeutique ?
Classe Chimique ?
Mécanisme d'action ?
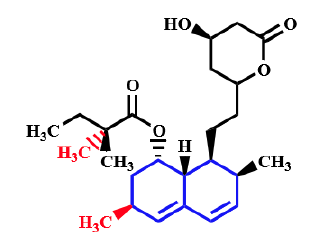
Simvastatine - Classe Thérapeutique : Normolipémiant hypolipémiant
Classe Chimique : Inhibiteurs de l’HMG Co-A réductase (Statines)
Mécanisme d'action :Les statines vont agir en bloquant la synthèse de cholestérol à partir de l’Acétyl-CoA.
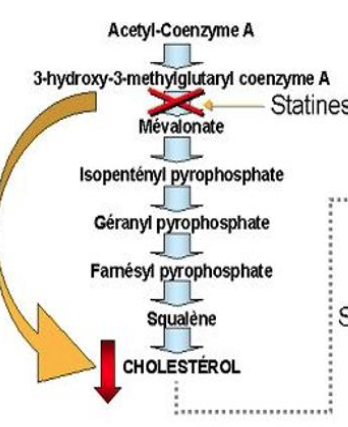
Classe Thérapeutique ?
Classe Chimique ?
Mécanisme d'action ?
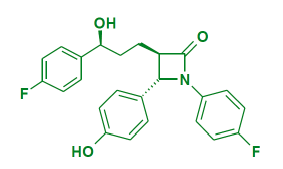
Ézétimibe - Classe Thérapeutique : Normolipémiant hypolipémiant
Classe Chimique : Inhibiteurs de l’absorption du Cholestérol
Mécanisme d'action : Inhibe le transport du cholestérol au niveau de l’entérocyte, en association avec une statine pour abaisser plus efficacement les LDL, cible : protОine Niemann-Pick C1-Like 1 (NPC1L1), facteur clé de l’absorption du cholestérol
Classe Thérapeutique ?
Mécanisme d'action ?
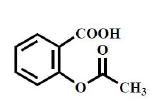
Aspirine - Classe Thérapeutique : Antiagrégant plaquettaire = antithrombine
Mécanisme d'action : Inhibiteur de cyclo-oxygénase
- inh synth prostalandines pro-inflammatoires Cox endothéliale
- Inh synth thromboxane A2 Cox plaquettaire
A faible dose ratio en faveur inh TX A2 --> anti agrégrant plaquettaire
Classe Thérapeutique ?
Mécanisme d'action ?
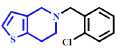
Ticlopidine - Classe Thérapeutique : Antiagrégant plaquettaire = antithrombine
Famille Chimique : Thiénopyridines
Mécanisme d'action : bloquent, de manière irréversible, les récepteurs à l’ADP présents sur les plaquettes (P2Y12)
Métabolisme ; la Ticlopidine, le Clopidogrel et le Prasugrel sont d'abord présentés sous la forme de prodrogues inactives. Leur activation nécessite deux étapes ;
Dans le cas des deux premières molécules, c'est une étape d'oxydation par une CYP450, et pour le Prasugrel, c'est une étape d'hydrolyse par une estérase.
Dans les trois cas, il s'agit d'une oxydation par une CYP450 qui va ouvrir le thiophène
et laisser apparaître une fonction SH et une fonction COOH.
On peut citer comme autre antagoniste REVERSIBLES des récepteurs à l’ADP P2Y12 le Ticagrelor et le Cangrelor tetrasodique.
Classe Thérapeutique ?
Mécanisme d'action ?
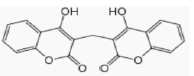
Dicoumarol - Principes actifs sur les facteurs de la Coagulation
- PA modifiant la synthèse des facteurs de la Coag.
Famille : Anti-vitamine K
Classe Thérapeutique ?
Mécanisme d'action ?
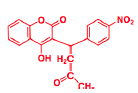
Acénocoumarol - Principes actifs sur les facteurs de la Coagulation
PA modifiant la synthèse des facteurs de la Coag.
Famille : Anti-vitamine K
Classe Thérapeutique ?
Mécanisme d'action ?
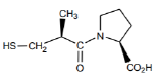
Captopril - Inhibiteur de l'enzyme de conversion
Antihypertenseur
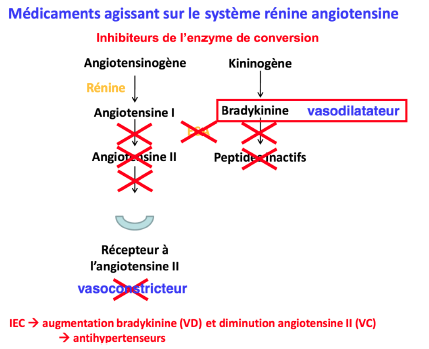
Comment optimiser le captopril ?

1) Occuper la poche S1 mais attention dans tout les cas, il faut complexer l’atome Zn2+
2) Occuper au maximum la poche qu’occupe la proline (S’2)
3) Bloquer l’isomérie s-cis/s-trans de l’amide (le s correspond à liaison sigma)
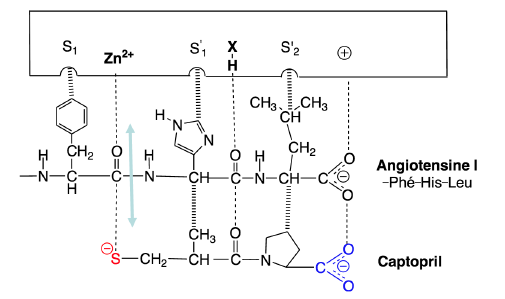
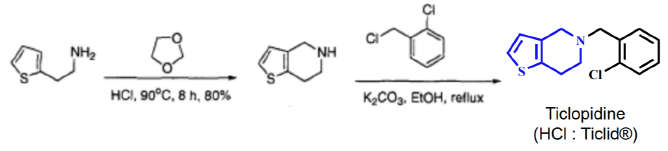
Le premier composé, le formaldéhyde, résulte d’une hydrolyse de l’acétal en milieu acide. C’est un composé très toxique car il forme des adduits avec l’ADN et les protéines. En effet, c’est un composé à caractère réducteur majoritairement mais cela dépend du composé qu’il a en face, il s’oxyde donc pour former l’acide formique.
3-4-5 sont des intermédiaires réactionnels corrélés obtenus par une autre voie de synthèse. 7 est à rechercher comme impureté, la substitution électrophile se fait sur un autre site, le cycle se forme des deux côtés. 8 = produit 1 + dernier réactif. Le dernier produit est un isomПre de la Ticlopidine. L’avant dernier composé est toujours une impureté
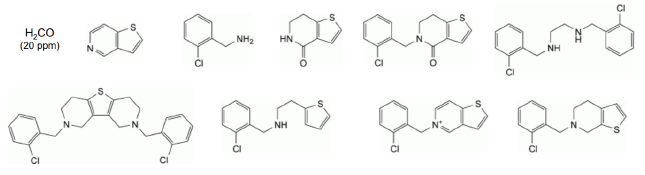
Comment contrôler la molécule/la pureté du produit final ?
- Contrôle de l’avant dernier composé de synthèse
- Contrôle des produits de départs
- contrôle du pouvoir rotatoire
l’action des différents récepteurs
- Récepteur ɑ1 :
- Récepteur ɑ2 :
- Récepteur β1 :
- Récepteur β2 :
- Récepteur ɑ1 : contraction muscles lisses
- Récepteur ɑ2 : régulation de la libération de Noradrénaline
- Récepteur β1 : fonction cardiaque
- Récepteur β2 : relaxation musculaire lisse
Citez une méthode de dosage qui n’est pas physico-chimique.
Donc à partir du moment où on est en présence d’une molécule qui absorbe dans l’UV, on pourra faire le dosage de cette molécule par une chromatographie liquide ou gazeuse (méthode séparative) couplée à une détection UV. C’est une méthode physico-chimique. On peut également utiliser, dans le cas des acides, une méthode chimique, avec un dosage par une base (ex : CH3Oli ou NaOH).
Classe Thérapeutique ?
Classe Chimique ?
Cible ?
Mécanisme d'action ?

amorolfine - Classe Thérapeutique : Antifongiques de synthèse
Classe Chimique : AUTRES ANTIFONGIQUES A ACTION topique
Mécanisme d'action : elle agit après la différenciation du lanostérol donc sur 2 enzymes : une réductase et une isomérase, provoque donc une perturbationde la synthèse de l’ergostérol et donc de la paroi cellulaire des champignons.
Classe thérapeutique ?
Famille chimique ?
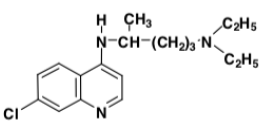
Chloroquine - Classe thérapeutique : Antiparasitaire -
Famille Chimique : Chef de fil : antipaludique - Schizonticides sanguins à action rapide : Quinine et Chloroquine
Classe thérapeutique ?
Famille chimique ?
Amodaquine - Classe thérapeutique : Antiparasitaire -
Famille Chimique : antipaludique - Schizonticides sanguins à action rapide : Quinine et Chloroquine
Justifier le caractère dibasique de la Chloroquine
Dibasique : pKa : 10,2 (amine tertiaire) et pKa : 8,1 (pyridine)
Malgré le fait que nous avons 3 azotes, cette molécule ne possède que 2 pKa : correspondant à l’amine tertiaire et l’autre par l’équilibre de la charge positive entre l’azote extracyclique et l’azote intracyclique. (En gros qu’une seule valeur de pKa pour les deux azotes du cycle selon la stabilisation par la charge positive, il y aura donc qu’un seul azote pourra se protonner).
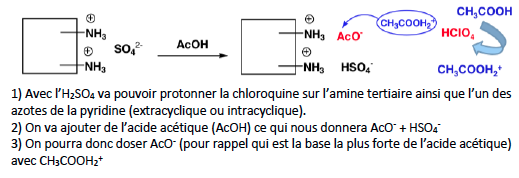
Qu'est-ce qu'un solvant amphitrophiques ?
protophiles et protogéniques
Protométrie en milieu non aqueux
Décrire les interaction entre la Quinine et l'hémine
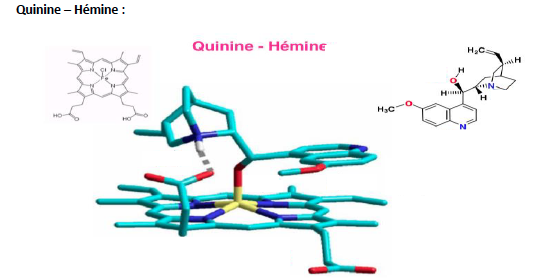
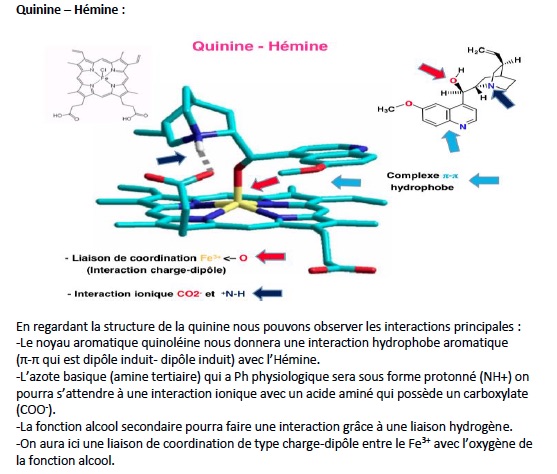
Dosage Quinine
Jusifier
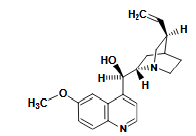
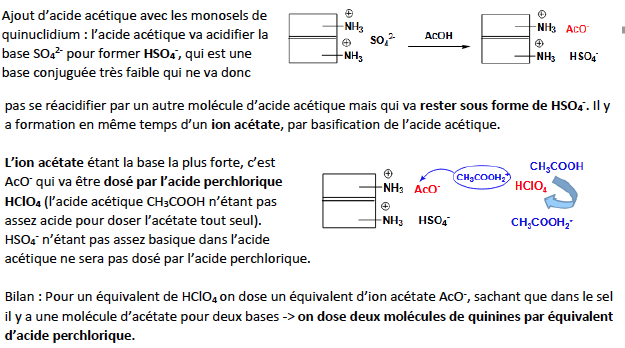
Caractères chimiques de la quinine
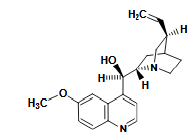
Quinuclidine N (sp3) : pKa = 9,7
Quinoléine N (sp2) : pKa = 5,07 (pas assez basique pour réagir avec un acide)
H2SO4 possède 2 protons acides : Donc il est capable de transférer 2 protons à la quinine, mais il n’y a que l’azote quinuclidinique qui va être acidifié (le deuxième azote n’étant pas assez basique pour capter un proton). Une molécule de H2SO4 est donc capable d’acidifier deux molécules de quinine.
Classe thérapeutique ?
Famille Chimique ?

Quinine - Classe thérapeutique : Antiparasitaire -
Famille Chimique : antipaludique - Schizonticides sanguins à action rapide : Quinine et Chloroquine
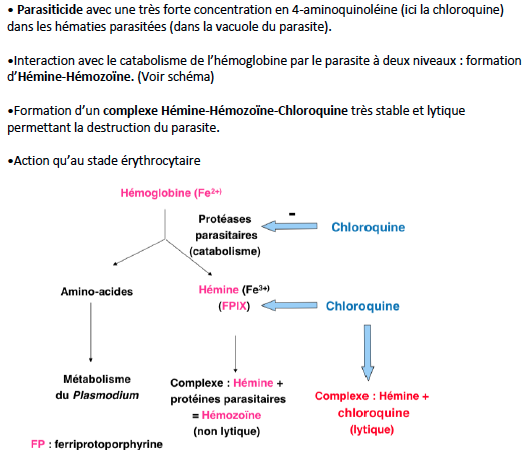
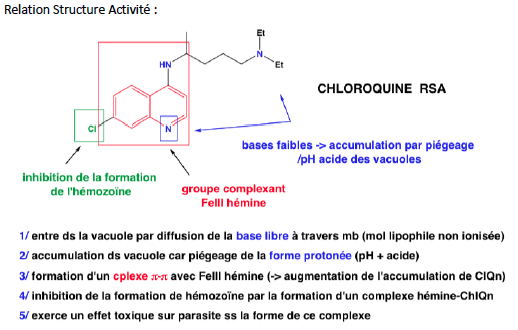
Décrire les intéraction entre l'hémine et la chloroquine
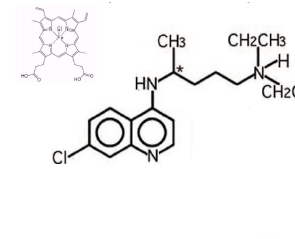
Classe thérapeutique : Antiparasitaire -
Famille Chimique : antipaludique - Schizonticides sanguins à action rapide : Quinine et Chloroquine
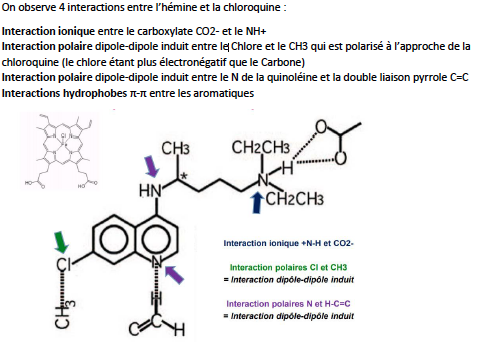
Classe thérapeutique ?
mécanisme d'action
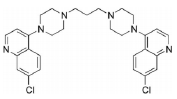
Pipéraquine - Son mécanisme d'action est identique à la chloroquine. Cependant elle est active sur les souches de Plasmodium résistantes à la chloroquine par inhibition des transporteurs qui assurent l'exocytose de Chloroquine à partir des vacuoles digestives du parasite Elle est utilisée en association avec arténimol = dihydroartemisinine pour les paludismes non compliqués Pl. falciparum.
Même mécanisme d’action que la chloroquine. Elle détruit les formes asexuées et ses cibles ne sont pas connues.
Classe thérapeutique ?
Famille Chimique ?
Mécanisme d’action ?
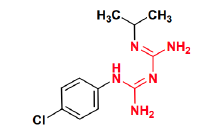
PROGUANIL - Classe thérapeutique : Antiparasitaire -Antimétabolites à action lente
Famille Chimique : INHIBITEURS DE LA DIHYDROFOLATE REDUCTASE
Mécanisme d’action :
Il s’agit d’une prodrogue dont l’activation est hépatique par le CYP450. On obtient un dérivé
cyclique de la dihydrotriazine.
C’est un inhibiteur spécifique de la dihydrofolate réductase du parasite.
La dihydrofolate réductase réduit l’Acide dihydrofolique en acide tétrahydrofolique qui est
un cofacteur de synthèse des bases puriques.
ASSOCIATION SULFAMIDE ANTIFOLIQUE et INHIBITEURS DE LA
DIHYDROFOLATE REDUCTASE : SULFADOXINE + PYRIMETHAMINE
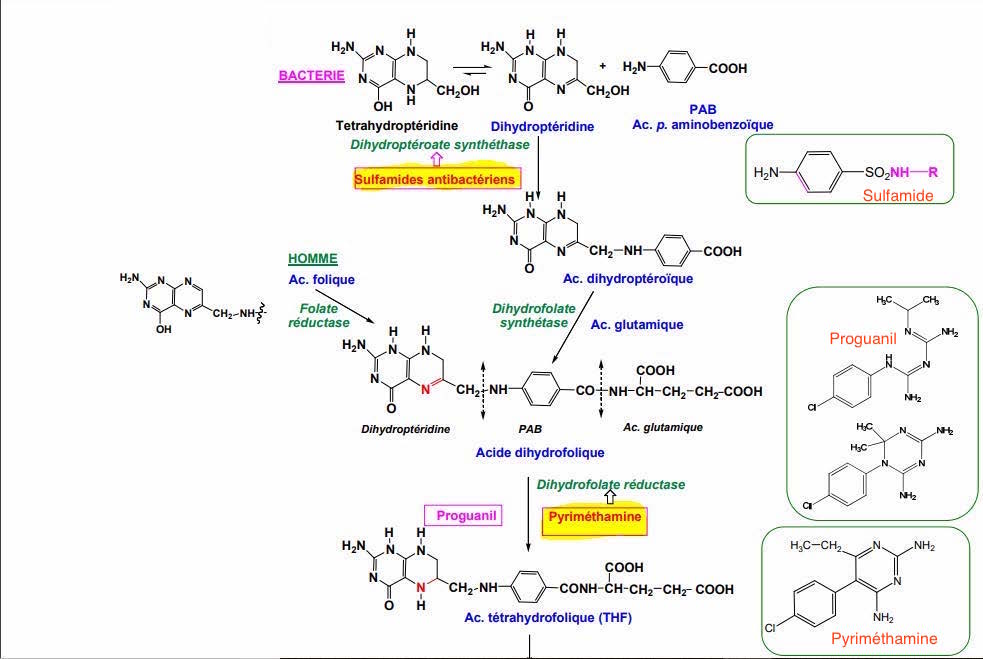
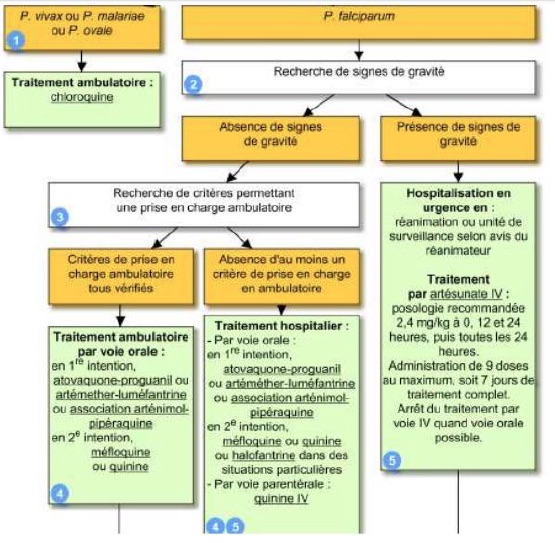
Traitement Infection palustre
Classe thérapeutique ?
Classe chimique ?
Mécanisme d'action ?
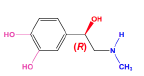
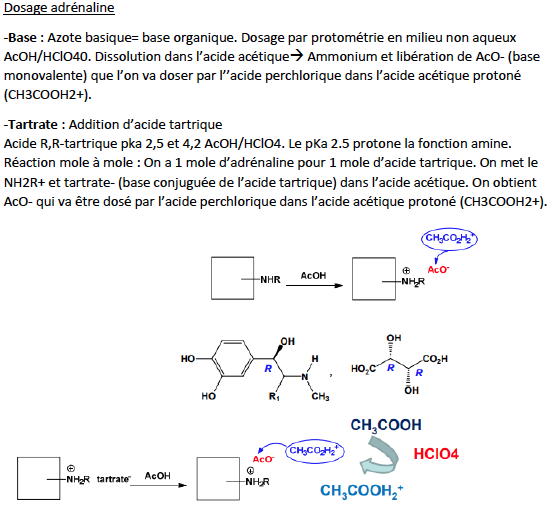
Adrénaline - Classe thérapeutique : Etant donné qu’elle est en NH(CH₃), elle permettra l’activation des récepteurs ɑ et des récepteurs β. Elle n’est pas spécifique.
Elle a un effet hypertenseur et légèrement bronchodilatateur (β2).
- traitement de choix en urgence pour choc anaphylactique
- arrêt cardiaque
- traitement du glaucome à angle ouvert
- aérosol bronchodilatateur pour l’asthme (plus maintenant)
Classe chimique : Catéchol - Amino-Alcools sympathomimétiques
Mécanisme d'action : On observe donc une interaction molécule-récepteur avec 3 points de contact (il s’agit d’interactions polaires).
Interaction ionique avec l’amine protonée (NH⁺ à pH basique) et un acide aminé chargé négativement : Acide aspartique (Aspartate présent sur le domaine transmembranaire 3) car à pH physiologique, l’acide carboxylique sera majoritairement déprotoné sous forme COO¯.
Liaison hydrogène avec la fonction hydroxyle avec un acide aminé qui sera l’asparagine (CH2- CO-NH2 présent sur le domaine transmembranaire 6)
Liaison hydrogène des deux –OH du noyau aromatique avec deux Sérines (présentes sur les
domaines transmembranaires 5)

Classe thérapeutique ?
Classe chimique ?
Mécanisme d'action ?
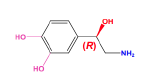
Noradrénaline - Classe thérapeutique :
Récepteur ɑ +++ (R2 = NH2)
Indications thérapeutiques : Analeptique vasculaire Utilisée dans :
- - les collapsus vasculaires liés à une baisse brutale du tonus vasomoteur périphérique (choc anaphylactique)
- - dans les états de choc hémorragique ou cardiogénique
Classe chimique : Catéchol - Amino-Alcools sympathomimétiques
Mécanisme d'action : On observe donc une interaction molécule-récepteur avec 3 points de contact (il s’agit d’interactions polaires).
Interaction ionique avec l’amine protonée (NH⁺ à pH basique) et un acide aminé chargé négativement : Acide aspartique (Aspartate présent sur le domaine transmembranaire 3) car à pH physiologique, l’acide carboxylique sera majoritairement déprotoné sous forme COO¯.
Liaison hydrogène avec la fonction hydroxyle avec un acide aminé qui sera l’asparagine (CH2- CO-NH2 présent sur le domaine transmembranaire 6)
Liaison hydrogène des deux –OH du noyau aromatique avec deux Sérines (présentes sur les
domaines transmembranaires 5)
Classe thérapeutique ?
Classe chimique ?
Mécanisme d'action ?
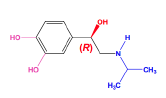
Isoprénaline - Classe thérapeutique : Récepteurs β (β1 et β2)
On aura donc un effet cardiaque grâce aux récepteurs β1. On aura également un effet bronchodilatateur intense grâce aux récepteurs β2 (x10 par rapport à de l’adrénaline).
Indications thérapeutiques :
- Traitement des troubles de la conductibilité auriculo-ventriculaire (dromotrope +)
- Traitement des états de choc
- Traitement de l’asthme (avant) (propriétés bronchodilatatrices mais effet β1 donc palpitation et tachycardie) -> Donc recherche de β2 agissant uniquement sur les bronches et pas sur le cœur. Recherche d’une meilleure spécificité.
Classe chimique : Catéchol - Amino-Alcools sympathomimétiques
Mécanisme d'action : On observe donc une interaction molécule-récepteur avec 3 points de contact (il s’agit d’interactions polaires).
Interaction ionique avec l’amine protonée (NH⁺ à pH basique) et un acide aminé chargé négativement : Acide aspartique (Aspartate présent sur le domaine transmembranaire 3) car à pH physiologique, l’acide carboxylique sera majoritairement déprotoné sous forme COO¯.
Liaison hydrogène avec la fonction hydroxyle avec un acide aminé qui sera l’asparagine (CH2- CO-NH2 présent sur le domaine transmembranaire 6)
Liaison hydrogène des deux –OH du noyau aromatique avec deux Sérines (présentes sur les
domaines transmembranaires 5)
Classe thérapeutique ?
Classe chimique ?
Mécanisme d'action ?
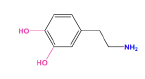
Dopamine - Classe thérapeutique : Absence d’alcool secondaire sur la dopamine. Elle agit sur les récepteurs adrénergiques ɑ et β, également sur les récepteurs dopaminergiques.
Dans l’ensemble, les catécholamines peuvent être utilisées à des fins thérapeutiques différentes :
- vasodilatation
- vasoconstriction
- bronchodilatation
Indications thérapeutiques :
Traitement des troubles de la conductibilité auriculo-ventriculaire (dromotrope +)
Traitement des états de choc
Traitement de l’asthme (avant) (propriétés bronchodilatatrices mais effet β1 donc palpitation et tachycardie) -> Donc recherche de β2 agissant uniquement sur les bronches et pas sur le cœur. Recherche d’une meilleure spécificité.
Classe chimique : Catéchol - Amino-Alcools sympathomimétiques
Mécanisme d'action : On observe donc une interaction molécule-récepteur avec 3 points de contact (il s’agit d’interactions polaires).
Interaction ionique avec l’amine protonée (NH⁺ à pH basique) et un acide aminé chargé négativement : Acide aspartique (Aspartate présent sur le domaine transmembranaire 3) car à pH physiologique, l’acide carboxylique sera majoritairement déprotoné sous forme COO¯.
Liaison hydrogène avec la fonction hydroxyle avec un acide aminé qui sera l’asparagine (CH2- CO-NH2 présent sur le domaine transmembranaire 6)
Liaison hydrogène des deux –OH du noyau aromatique avec deux Sérines (présentes sur les
domaines transmembranaires 5)
recepteur ?
Indication thérapeutique ?
Famille Chimique ?
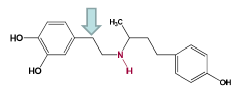
Dobutamine - pas de –OH mais groupement sur l’azote :
Stimulation récepteur β et plus particulièrement des β1 cardiaques -> augmentation du dОbit cardiaque.
Indications thérapeutiques :
• Traitement des Оtats caractérisés par un débit cardiaque bas : infarctus, Оtat de choc, embolies pulmonaires graves
• Perfusion IV lente
Famille Chimique : Analogues des catécholamines de type Dopamine
Recepteurs ?
Indication thérapeutique ?
Famille Chimique ?
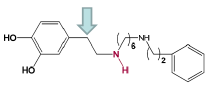
Dopexamine - Action sur récepteur β2 et récepteurs dopaminergiques D1 et D2.
Indications thérapeutiques :
Traitement à court terme des poussées aiguës de l’insuffisance cardiaque chronique congestive
Traitement du syndrome de bas débit en chirurgie cardiaque
Famille Chimique : Analogues des catécholamines de type Dopamine
Recepteurs ?
Indication thérapeutique ?
Famille Chimique ?
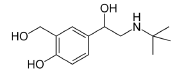
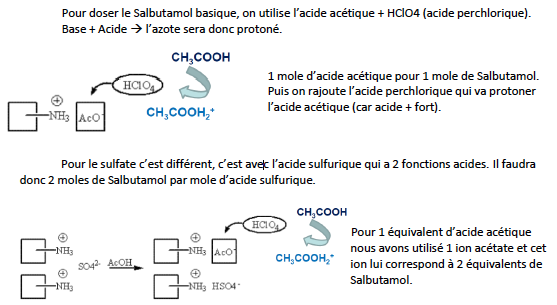
Salbutamol - Ici, on a une très grande sélectivité β2. Un des hydroxyles phénoliques remplacé par un alcool.
Indications thérapeutiques :
- Bronchodilatateur
- Effet plus spécifique et plus prolongé que l’Isoprénaline
- Traitement de l’asthme et de l’emphysème pulmonaire
L’asthme : affection bronchique de plus en plus fréquente avec obstruction des bronches et phénomène inflammatoire (300 millions dans le monde) :
- Peut conduire à une Broncho Pneumopathie Obstructive Evolutive (BPCO) à détérioration définitive
des capacités respiratoires - France : 2 millions d’asthmatiques et 2000 morts /an Cependant, on n’utilise pas d’agonistes β de façon régulière sans une association avec d’autres antiasthmatiques qui traitent l’inflammation (comme les corticoïdes).
Famille Chimique : Analogues des catécholamines Dérivés à hydroxyle modifié
Recepteurs ?
Indication thérapeutique ?
Famille Chimique ?
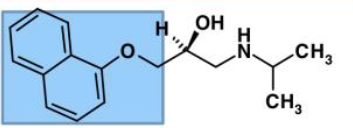
propranolol - Recepteurs : Antagoniste compétitifs réversibles des catecholamines au niveau des recepteurs β Adrenergiques
Indication thérapeutique :
Cardiaques, bronchiques et vasculaires (pour les premiers)
l’objectif étant soustraire le cœur à l’action des catecholamines. Ces molecules vont venir s’opposer à la tachycardie et à l’augmentation du travail cardiaque provoquées par les catécholamines. Il va donc y avoir
diminution du débit cardiaque et diminution des besoins en O2 du myocarde.
Action sur N isop ou tBu
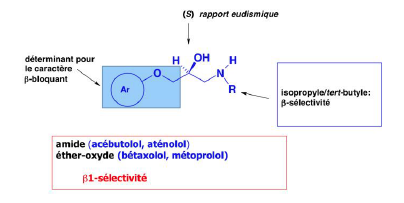
- certains sont cardiosélectifs car ils sont antagonistes β1 cardiaque >> β2
Concerne ceux qui sont substitués en position para sur le noyau Ar avec C=O ou éther sur chaine Ar.
ex : acébutolol, aténolol, métoprolol, bétaxolol
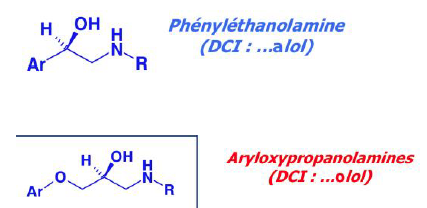
Famille Chimique : Aryloxypropanolamine
Usage : HTA, angine de poitrine (angor), trouble rythme cardiauqe, infarctus du myocarde, IC chronique, migraine, anesthésiologie, hypertonie intraoculaire!
•Polycycliques (ex propranolol)
•Monocyclique ortho substitué
•Monocyclique para substitué
•Monocyclique ortho et para substitués
•Polycycliques (ex propranolol) β1 + β2 sans ou avec ASI
•Monocyclique ortho substituО β1 + β2 avec ASI
•Monocyclique para substituО β1 sans ASI
•Monocyclique ortho et para substituОs β1 avec ASI
Rapport eudismique ?
Rapport eudismique : rapport d’efficacité des 2
énantiomères
On peut voir que pour le propranolol le ER
(rapport eudismique) est égal à 130. Soit
l’énantiomère S est 130 fois plus actif que
l’énantiomère R.
ß bloquants
Plusieurs catégories d’antagonistes calciques :
- 1/Les Dihydropyridines : ?
- 2/Le Vérapamil : ?
- 3/Le Diltiazem : ?
- 4/Le Bepridil : ?
Plusieurs catégories d’antagonistes calciques :
- 1/Les Dihydropyridines : effet vasculaire prédominant.
- 2/Le Vérapamil : effet cardiaque prédominant.
- 3/Le Diltiazem : effet mixte : cardiaque et vasculaire.
- 4/Le Bepridil : il n’est pas sélectif des canaux calciques lents.
Classe thérapeutique :
classe chimique :
mécanisme d'action :
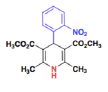
Nifédipine - Classe thérapeutique : antiangoreux
classe chimique : Dihydropyridines : effet vasculaire prédominant.
mécanisme d'action : antagonistes calciques
-Mécanisme d’action : on a une inhibition du passage transmembranaire du Ca2+ par les canaux
calciques lents donc une diminution du calcium intracellulaire et un effet antispasmodique sur les fibres musculaires lisses.
-Implication : Au niveau du cœur, on a une diminution de la force de contraction sauf pour la
lacidipine. Cependant, ce qui est principalement recherché c’est l’activité au niveau vasculaire. On a donc une relaxation musculaire au niveau des artères ce qui conduit à une vasodilatation
artérielle. L’effet vasculaire est prédominant et extrêmement intense sur l’artère coronaire. De
plus, on a un effet antiangoreux avec une diminution des besoins en O2 du myocarde.
Classe thérapeutique ?
Mécanisme d'action ?
Propriétés pharmacologiques ?
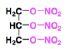
Trinitrine - Classe thérapeutique : Antiangoreux
Mécanisme d'action :
Les dérivés nitrés vont être des donneurs de radical NO°. En ce qui concerne le NO° physiologique,
il y a une oxydation enzymatique d’un des azotes du groupe guadinidium de l’arginine pour aboutir à une citrulline par la NO synthase.
Le radical NO° va être actif sur la guanylate cyclase, il y aura donc une production de GMPc à partir de GTP ce qui provoquera la relaxation de la fibre musculaire lisse par baisse du calcium libreintracellulaire.
Propriétés pharmacologiques :
Au niveau de l’appareil cardio-vasculaire, les dérivés nitrés ont une action anti-angineuse. Ils ontaussi un effet coronaro-dilatateur qui est dû à un effet direct sur les fibres musculaires lissesvasculaires.
Activité thérapeutique :
Action cardio-vasculaire : la trinitrine possède un effet relaxant direct sur le muscle lisse et est à l’origine d’une vasodilatation veineuse et artérielle, d’une amélioration du travail cardiaque et d’une diminution des besoins en O2 du cœur (effet anti-angineux).
Indications :
- -Traitement curatif de la crise d’angine de poitrine.
- -Traitement préventif à court terme de la crise angineuse.
- -Oedème aigu du poumon.
Les moyens thérapeutiques pour diminuer ou inhiber l’action de la sécrétion acide
Anti-acides ou neutralisants et topiques
Antisécrétoires (toujours prescrits en cas d’ulcère) avec :
- Des inhibiteurs des récepteurs de la cellule pariétale : les anticholinergiques (abandonnés car trop d’effets indésirables) et les antagonistes des R H2 de l’histamine = anti H2 = Cimétidine
- Des inhibiteurs de la pompe à protons = IPP
- - Cytoprotecteurs = PG
Emplois
Indication thérapeutique
Effets indésirables ?
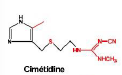
Cimétidine - Activité pharmacologique : antiulcéreux > Antisécrétoires> antagoniste Compétitif R H2, ils permettent l’inhibition de l’acidité gastrique.
Indications thérapeutiques :
Ulcère duodénal = indication type, cicatrisation dans 90% des cas après 6 semaines de traitement
Ulcère gastrique : taux de cicatrisation plus faible
Syndrome de Zollinger-Ellison : réduction de l’hypersécrétion
Complications hémorragiques des ulcères gastro-duodénaux
Modalités d’emploi et inconvénients de la CIMETIDINE : Administration par voie orale le plus souvent, voie parentérale lorsque l’on peut faire des formes solubles dans l’eau.
Effets indésirables :
Troubles neuropsychiques : vertiges, états confusionnels surtout chez les sujets âgés et quand IR
Troubles cutanés (prurit, érythème, éruptions)
Troublesendocriniens (inhibitionde lafixation de ladihydrotestostérone sur ses récepteurs, problème dans 0,3 % des cas : gynécomastie et impuissance (H), galactorrhée (F))
Troubles hématologiques (neutropénie,thrombocytopénie)
Bradycardie
Classe thérapeutique
Mécanisme d'action
Indication thérapeutique
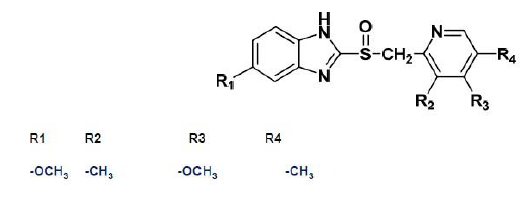
Oméoprazole - Classe thérapeutique : antiulcéreux > Antisécrétoires > inhibiteurs de la pompe à protons
Mécanisme d'action : Inhibition de la pompe à protonqui est l’effecteur terminal de la sécrétion d’acide gastrique.
C’est un effet inhibiteur quel que soit l’effet de la stimulation.
L’Oméprazole et tous les autres IPP sont des pro-drogues. Ils sont administrés sous forme de granules gastro-résistants car ils sont transformés en forme active en milieu acide mais cette transformation doit se faire exactement au niveau de la pompe à protons. Si la forme n’était pas gastro-résistante, le médicament qui passe d’abord dans l’estomac (qui est acide) sera alors transformé en composé actif au milieu de l’estomac ce qui ne servirait à rien. La molécule doit être absorbée par l’intestin grêle sous sa forme oméprazole (la pro-drogue), puis véhiculée par voie sanguine jusqu’à la cellule pariétale gastrique où elle s’accumule sous forme protonée (le pH étant acide). Elle peut alors être métabolisée en composé actif : le sulfénamide pour réagir avec la pompe à protons. Lesulfénamide va réagir avec les cystéines de la pompeà protons : formationde disulfure S-S.
L’enzyme est alors inhibée par liaison covalente : inhibition irréversible totale.
Indication thérapeutique : Ulcère duodénal ou gastique + efficace de ranitidine ; oesophagite à RGO , syndrome de Zollinger-Ellison
Citer 5 classes de médicaments
- Biguanides
- Insulino-sécréteurs
- Les gluco-intégrines
- Inhibiteurs des α-glucosidases
- Médicaments de l’insulinorésistance
Classe thérapeutique
Classe chimique
Mécanisme d'action
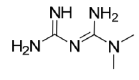
Metformine - Classe thérapeutique : médicaments du diabète de type 2 normoglycémiante
Classe chimique : Biguanide
Mécanisme d'action : La Metformine est normoglycémiante donc pas de risque d’hypoglycémie ! Elle agit en diminuant la néoglucogenèse hépatique. Elle améliore également l’utilisation périphérique du glucose et diminue probablement l’absorption intestinale du glucose. Enfin, elle est anorexigène et hypolipidémiante
- Absorption hépatique de la metformine par transporteur de cation organique OCT1
Mitochondrie = cible primaire (site de liaison non connu)
-> Inhibition spécifique du complexe I de la chaîne respiratoire (NADH/ubiquinone oxydoréductase)
-> Diminution de l’ATP cellulaire et augmentation concomitante de l’AMP
Néoglucogenèse = processus coûteux en énergie
-> Flux gluconéogénique restreint
Accumulation de AMP
-> Régulation allostérique de la F-1,6-BPhophatase
-> Réduction de l’activité de l’adénylate cyclase stimulée par le glucagon (hormone hyperglycémiante impliquée dans l’homéostasie)
-> Inhibition de la production de glucose par le foie
Classe thérapeutique
Classe chimique
Mécanisme d'action
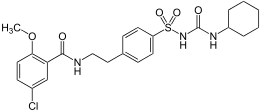
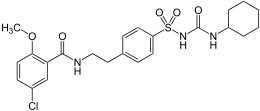
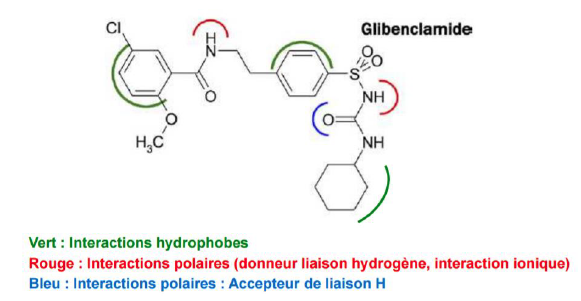
Glibenclamide - Classe thérapeutique : médicaments du diabète de type 2 Insulino-sécréteurs
Classe chimique : Sulfamides hypoglycémiants = Sulfonylurées
Mécanisme d’action :
Ces molécules agissent sur les canaux potassiques.
L’ouverture de ces canaux K+ ATP-dépendants va favoriser la sortie du K+, entraînant une hyperpolarisation, puis une diminution de l’entrée de calcium dans la cellule. Tout cela entraîne une relaxation des muscles lisses mais surtout la diminution de la sécrétion d’insuline.
La fermeture des canaux Katp conduit à des effets inverses : induction de la sécrétion d’insuline, ainsi que l’augmentation de la durée du potentiel d’action cardiaque.
Les antagonistes des canaux Katp sont donc des antidiabétiques mais aussi des anti-arythmiques.
Au niveau des cellules β du pancréas, la fermeture des canaux K+ ATP-dep va entraîner une hausse
de la [K+]IC. De plus, l’ouverture des canaux Ca2+ voltage-dep va entraîner la sécrétion d’insuline. Les sulfonylurées se lient sur les récepteurs de type 1 (SUR1)/ Ils sont membres de la superfamille des transporteurs ABC.
Ce sont des protéines transmembranaires avec un domaine de liaison de nucléotides capables
d’hydrolyser l’ATP.
Classe thérapeutique
Classe chimique
Mécanisme d'action
Classe thérapeutique : médicaments du diabète de type 2 Insulino-sécréteurs
Classe chimique : Glinides
Mécanisme d’action :
Ces molécules agissent sur les canaux potassiques.
L’ouverture de ces canaux K+ ATP-dépendants va favoriser la sortie du K+, entraînant une hyperpolarisation, puis une diminution de l’entrée de calcium dans la cellule. Tout cela entraîne une relaxation des muscles lisses mais surtout la diminution de la sécrétion d’insuline.
La fermeture des canaux Katp conduit à des effets inverses : induction de la sécrétion d’insuline, ainsi que l’augmentation de la durée du potentiel d’action cardiaque.
Les antagonistes des canaux Katp sont donc des antidiabétiques mais aussi des anti-arythmiques.
Au niveau des cellules β du pancréas, la fermeture des canaux K+ ATP-dep va entraîner une hausse
de la [K+]IC. De plus, l’ouverture des canaux Ca2+ voltage-dep va entraîner la sécrétion d’insuline. Les sulfonylurées se lient sur les récepteurs de type 1 (SUR1)/ Ils sont membres de la superfamille des transporteurs ABC.
Ce sont des protéines transmembranaires avec un domaine de liaison de nucléotides capables
d’hydrolyser l’ATP.
Deux voies thérapeutiques
Classe thérapeutique : médicaments du diabète de type 2 Insulino-sécréteurs
Classe chimique : gluco-intégrines
Mécanisme d’action :
Les incrétines (GLP1) sont des polypeptides pas très solides et dégradés par une enzyme : la DPP-4. Ils entraînent la sécrétion d’insuline en agissant au niveau du tube digestif.
Les gluco-intégrines sont des hormones polypeptidiques produites par le tractus gastro-intestinal en réponse à une prise alimentaire
Dans le DT2, on a observé une baisse très significative des taux circulants de GLP1, mais l’effet insulinotrope est conservé (l’effet du GLP-1 reste le même)
Deux voies thérapeutiques : soit inhiber les DPP-4 (Gliptines), soit administrer des analogues de GLP-1 (exanides).
Exemple de molécule
Mécanisme d'action
Ascarbiol
Mécanisme d'action :
Ils appartiennent à la classe des iminosucres
= glycomimétiques.
Ils agissent en régularisant la digestion et l’absorption des glucides.
Ils inhibent les α-glucosidases (inhibition compétitive donc réversible).
Ils miment l’état de transition (cation oxonium-carbonium) observé au cours de la réaction d’hydrolyse du sucrose et ont un
effet modeste sur la glycémie.
Nom de molécule
Mécanisme d'action
Nom de Molécule : Glitazone
Mécanisme d'action :
Ils combattent l’insulinorésistance, améliorent voire normalisent la tolérance au glucose sans recourir à une hyperproduction d’insuline et réduisent l’hyperinsulinémie.
Les glitazones sont des agonistes des récepteurs PPARγ impliqués dans le contrôle de la différenciation préadipocytaire.
Il y existe une corrélation entre puissance de l’activité antidiabétique et affinité pour les PPARγ. Des agonistes de PPARγ de structure différente sont également antidiabétiques.
Les glitazones sont maintenant interdites en raison de leurs effets indésirables (prise de poids, risque
cardiaque, atteintes hépatiques ect…).